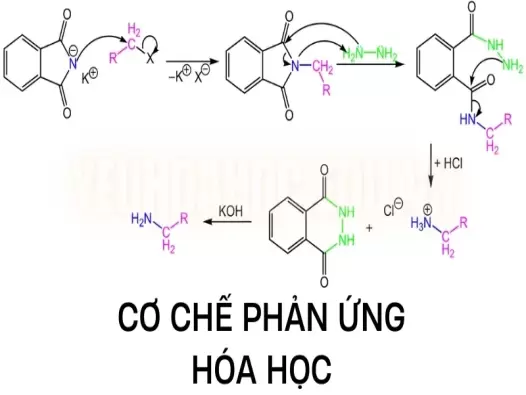
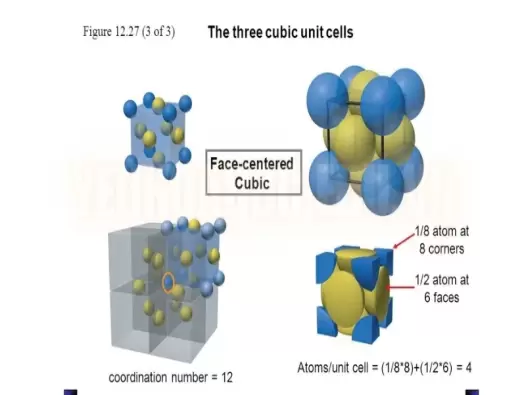
Phản ứng oxi hoá - khử: Sự trao đổi electron trong hóa học
Trong bài viết này chúng ta cùng tìm hiểu về phản ứng oxi hóa - khử, cách lập phương trình, các ví dụ cụ thể và ý nghĩa của chúng.
Phản ứng oxi hóa khử là một khía cạnh quan trọng trong hóa học, giúp chúng ta hiểu rõ về sự trao đổi electron giữa các chất tham gia phản ứng. Trong bài viết này yeuhoahoc.edu.vn sẽ cùng các bạn tìm hiểu về phản ứng oxi hóa khử, cách lập phương trình, các ví dụ cụ thể và ý nghĩa của chúng.
Phản ứng oxi hoá – khử là gì?
Phản ứng oxi hóa khử là quá trình trong đó một chất trao đổi electron với chất khác. Chất trao đổi electron bị oxi hóa, trong khi chất nhận electron bị khử. Quá trình này thường được biểu thị bằng sự thay đổi số oxi hóa của các nguyên tử hoặc ion trong phản ứng.
Các phản ứng oxi hoá – khử
Trong hoá học, các phản ứng oxi hóa khử có thể chia thành ba loại chính: phản ứng oxi hóa – khử thông thường, phản ứng oxi hóa – khử nội phân và phản ứng oxi hóa – khử tự nhiên.
Phản ứng oxi hóa – khử thông thường
Phản ứng này diễn ra khi một chất bị oxi hóa và mất electron (quy trình oxi hóa), trong khi chất khác nhận electron và bị khử (quy trình khử). Ví dụ:
Phản ứng oxi hóa – khử nội phân
Trong loại phản ứng này, cùng một chất tham gia phản ứng tự mình trao đổi electron và thay đổi số oxi hóa. Điều này thường xảy ra trong các quá trình điện hóa, chẳng hạn như trong pin điện hoá, khi nước chuyển thành oxy và hydro. Trong trường hợp này, nước được oxi hóa thành oxy và đồng thời hydrogen bị khử thành hydro.
Ví dụ:
Phản ứng ở cực anot (+):
Phản ứng catot (-):
⇒
Phản ứng oxi hóa – khử tự nhiên
Phản ứng oxi hóa – khử tự nhiên xảy ra khi các chất tham gia phản ứng trao đổi electron và thay đổi số oxi hóa mà không cần sự can thiệp của các chất hoá học khác. ( chất khử đồng thời là chất oxy hoá)
Ví dụ, quá trình oxi hóa của kim loại như sắt khi nó rỉ sét là một ví dụ về phản ứng oxi hóa – khử tự nhiên. Trong trường hợp này, sắt bị oxi hóa thành sắt oxit trong môi trường có nước và oxi, trong khi oxi bị khử.
Dấu hiệu nhận biết phản ứng oxi hoá – khử
Thay đổi Màu Sắc: Một trong những dấu hiệu rõ ràng của phản ứng oxi hóa khử là sự thay đổi màu sắc của các chất tham gia hoặc sản phẩm. Ví dụ, khi sắt rỉ sét, sắt ban đầu có màu bạc sẽ chuyển sang màu nâu sét.
Sự Thay Đổi Của Số Oxi Hóa: Trong quá trình phản ứng, số oxi hóa của các nguyên tử hoặc ion thay đổi. Sự tăng hoặc giảm số oxi hóa là một dấu hiệu rõ ràng của phản ứng oxi hóa khử.
Sự Tạo Ra Khí: Nếu khí được tạo ra trong quá trình phản ứng, đó có thể là một dấu hiệu. Ví dụ, trong phản ứng giữa sắt và axit clohydric, khí hidro được tạo ra và có thể thấy bong tróc khỏi dung dịch.
Sự Tạo Ra Nhiệt Độ: Một số phản ứng oxi hóa khử tạo ra nhiệt độ, tức là chúng tỏa nhiệt hoặc hấp thụ nhiệt trong quá trình phản ứng. Nếu bạn cảm thấy nhiệt độ tăng lên trong quá trình phản ứng, đó có thể là một dấu hiệu.
Thay Đổi Trạng Thái Vật Lý: Các sản phẩm có thể thay đổi trạng thái vật lý sau phản ứng. Ví dụ, một chất rắn có thể tan trong nước để tạo thành dung dịch, hoặc ngược lại, một dung dịch có thể kết tinh thành rắn.
Sự Thay Đổi Của pH: Nếu pH của dung dịch thay đổi trong quá trình phản ứng, đó cũng là một dấu hiệu. Ví dụ, khi kim loại reagieren với axit, pH thường giảm do tạo ra ion hydro và nước.
Ý nghĩa của phản ứng oxy hoá – khử
Phản ứng oxi hóa khử là một trong những loại phản ứng hóa học quan trọng nhất, đóng vai trò chủ đạo trong nhiều quá trình xảy ra trong tự nhiên và đời sống. Dưới đây là một số ý nghĩa quan trọng của phản ứng oxi hóa khử:
Năng lượng
Phản ứng oxi hóa khử là nguồn gốc của năng lượng cho hầu hết các hoạt động sống trên Trái Đất. Ví dụ:
- Quá trình hô hấp: Quá trình oxi hóa khử trong tế bào sinh vật giúp giải phóng năng lượng từ thức ăn để duy trì hoạt động sống.
- Đốt cháy nhiên liệu: Năng lượng được giải phóng từ phản ứng oxi hóa khử của nhiên liệu được sử dụng cho nhiều mục đích như: sưởi ấm, nấu nướng, vận tải, sản xuất điện,…
Luyện kim

- Quá trình khử được ứng dụng để điều chế kim loại từ quặng. Ví dụ:
- Sản xuất nhôm: Quá trình điện phân nóng chảy Al2O3 để thu được kim loại nhôm.
- Sản xuất thép: Quá trình khử quặng sắt bằng than cốc trong lò cao để thu được gang.
Hóa học hữu cơ
- Phản ứng oxi hóa khử đóng vai trò quan trọng trong nhiều phản ứng hóa học hữu cơ, ví dụ như:
- Quá trình đốt cháy: Phản ứng oxi hóa khử của các hợp chất hữu cơ.
- Phản ứng thế: Phản ứng oxi hóa khử xảy ra giữa các hợp chất hữu cơ.
Pin và acquy:
- Hoạt động của pin và acquy dựa trên nguyên tắc của phản ứng oxi hóa khử.
- Pin: Phản ứng oxi hóa khử xảy ra tự phát, tạo ra dòng điện.
- Acquy: Phản ứng oxi hóa khử xảy ra theo chiều ngược lại khi được nạp điện.
Xác định thành phần hóa học:
- Phản ứng oxi hóa khử được sử dụng để xác định thành phần hóa học của các chất.
Ví dụ: Phân tích định lượng là việc xác định nồng độ của một nguyên tố trong hợp chất sử dụng phương pháp chuẩn độ.
4 bước lập phương trình phản ứng oxi hoá – khử
Để lập phương trình phản ứng oxi hóa khử, ta cần thực hiện các bước sau:
Bước 1: Tìm và xác định số oxi hóa của các nguyên tố:
- Số oxi hóa là số điện tích mà nguyên tử đó mang khi nhường hoặc nhận electron.
- Một số nguyên tắc để xác định số oxi hóa bao gồm: Số oxi hóa của nguyên tố trong các đơn chất luôn là 0..
- Số oxi hóa của nguyên tố trong hợp chất bằng tổng số điện tích của các nguyên tử liên kết với nó.
- Số oxi hóa của H trong hợp chất với kim loại thường là +1.
- Số oxi hóa của O trong hợp chất với phi kim thường là -2.
Bước 2. Xác định nguyên tố oxi hóa và nguyên tố khử:
- Nguyên tố oxi hóa là nguyên tố nhận electron.
- Nguyên tố khử là nguyên tố nhường electron.
Bước 3. Cân bằng electron:
- Số electron mà nguyên tố khử nhường bằng số electron mà nguyên tố oxi hóa nhận.
- Cân bằng electron bằng cách thêm hệ số thích hợp vào các chất tham gia phản ứng.
Bước 4: Cân bằng phương trình:
- Cân bằng số nguyên tử của mỗi nguyên tố (trừ H và O) bằng cách thêm hệ số thích hợp vào các chất tham gia và sản phẩm.
- Sau khi cân bằng electron và số nguyên tử, kiểm tra lại xem phương trình đã cân bằng hay chưa.
Ví dụ:
Lập phương trình phản ứng:
Bước 1: Xác định số oxi hóa:
- Mg: 0 → +2
- H: +1 → 0
- Cl: 0 → -1
Bước 2: Xác định nguyên tố oxi hóa và nguyên tố khử:
- Mg là nguyên tố khử. Mg
- Cl là nguyên tố oxi hóa.
Bước 3: Cân bằng electron:
- Mg nhường 2 electron.
- Cl nhận 1 electron.
- Nhân chéo hệ số để cân bằng electron:
Mg + 2HCl → MgCl2 + H2
Đây là một ví dụ khác về phản ứng oxi hóa khử, trong đó hai chất tham gia phản ứng bị thay đổi số oxi hóa và tạo ra các sản phẩm mới.
Ví dụ về phản ứng oxy hoá – khử
Phản ứng đốt cháy
- Mg cháy trong khí oxi:
- Sắt cháy trong khí oxi:
- Cồn cháy trong không khí:
Phản ứng khử
- Khử oxit kim loại:
- Khử quặng kim loại:
Phản ứng thế
- Zn tác dụng với dung dịch HCl:
- Fe tác dụng với dung dịch CuSO4:
Phản ứng trong pin và acquy:
- Pin Zn – Cu:
- Acquy chì:
Phản ứng trong hô hấp
- Quá trình hô hấp:
Ngoài những ví dụ trên, còn có rất nhiều phản ứng oxi hóa khử khác xảy ra trong tự nhiên và đời sống.
Phản ứng oxi hóa khử là một loại phản ứng hóa học quan trọng, có vai trò thiết yếu trong nhiều lĩnh vực của đời sống và khoa học kỹ thuật.
Bài tập về phản ứng oxy hoá – khử
Ví dụ 1: Cho phương trình hóa học:
Xác định:
- Loại phản ứng hóa học.
- Chất khử, chất oxi hóa.
Cách giải:
- Xác định loại phản ứng hóa học:
- Số oxi hóa của Fe trong Fe là 0.
- Số oxi hóa của Fe trong
là +2. - Số oxi hóa của H trong HCl là +1.
- Số oxi hóa của H trong
là 0.
Vì số oxi hóa của Fe thay đổi từ 0 sang +2 nên phản ứng này là phản ứng oxi hóa – khử.
- Xác định chất khử, chất oxi hóa:
- Chất khử là Fe:
- Chất oxi hóa là HCl:
Ví dụ 2: Cho 13,44 gam hỗn hợp gồm Fe và Mg tác dụng với dung dịch HCl dư, thu được 6,72 lít khí hiđro (đktc). Xác định thành phần % khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
Tóm tắt: Fe + HCl dư
0,3mol
. %Fe = ?, %Mg = ?Mg
Cách giải:
Bước 1: Viết phương trình hóa học cân bằng.
Bước 2: Tính toán theo số mol.
- nH2 =
= 0,3 mol - Gọi số mol của Fe và Mg lần lượt là x và y.
- Theo phương trình hóa học:
(1)
- Khối lượng hỗn hợp kim loại:
= 13,44 gam = 56x + 24y = 13,44 (2)
- Từ (1) và (2) ta có hệ phương trình:
x + y = 0,3
56x + 24y = 13,44
- Giải hệ phương trình, ta được:
{x = 0,195}
{y = 0,105}
- Thành phần % khối lượng của mỗi kim loại:
%mFe =
%mMg = 100% – 81,25% = 18,75%